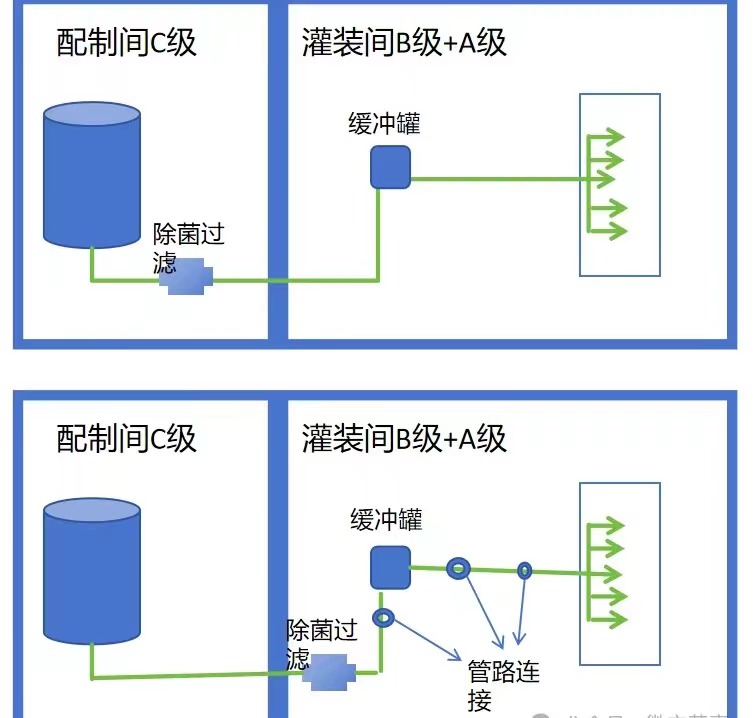
我的問題是下面兩個圖,哪個更符合“除菌過濾濾器應當盡可能接近灌裝點”?
在這之前,我們先看法規要求。歐盟附錄里的原文“Due to the potential additional risks of a sterile filtration process, an additional filtration through a sterile sterilising grade filer, as closed to the point of fill as possible, should be considered as part of an overall CCS.”
GMP 附錄1 第七十五條非最終滅菌產品的過濾除菌應當符合以下要求:(二)應當采取措施降低過濾除菌的風險。宜安裝第二只已滅菌的除菌過濾器再次過濾藥液,最終的除菌過濾濾器應當盡可能接近灌裝點。
問題:這里的接近灌裝點是物理距離上的接近嗎?
我們再來看看Ian的解釋,他說“closed”并不是物理距離上的接近,更多的是指除菌過濾后應盡量減少管路連接或者使用無菌連接。如果是無菌連接,一根較長的管道也可以看成“closed”。他認為學員提問里的檢查員可能母語不是英語,或者還沒有接受足夠的培訓沒有正確理解這句話。
我個人比較認同Ian的解釋,所以第一幅圖中第一個更能降低無菌風險。企業在做工序設計的時候應該盡量減少管路連接或者改成無菌連接,不要僅僅考慮距離上的接近。
聲明1、本公眾號的案例均為作者虛構,或者經過充分的再加工,所引用的數值也不是實際數值。如果仍然給某些企業帶來困擾,請與本號聯系進行刪除。2、本公眾號發布的文章均為促進制藥界同行的交流與學習。不用于任何商業用途。

原創 藥事